
RNA修饰在生命过程和疾病发生发展中的作用逐渐受到重视,其中5-甲基胞嘧啶(m5C)修饰是热门研究领域。
本文聚焦于m5C 甲基转移酶NSUN2在肝癌中的作用,NSUN2通过M5C修饰稳定PKM2 mRNA促进肝癌糖酵解和进展。
m5C修饰是指在RNA分子中,通过特定的酶将胞嘧啶(C)的第5位碳原子上加上一个甲基基团,形成5-甲基胞嘧啶。
这种修饰不会改变RNA的基本核苷酸序列,但会在不改变遗传信息编码的基础上,赋予RNA新的化学和生物学特性。
m5C修饰主要由NSUN(NOL1/NOP2/SUN)家族的甲基转移酶催化完成,涉及mRNA稳定性与翻译调控、tRNA 稳定性与解码功能、
rRNA加工与核糖体功能和非编码RNA功能调节,广泛地参与到各种生命活动的调控中。
研究背景:
肝癌(HCC)是常见癌症及癌症死亡主要原因,术后转移复发致患者5年生存率低。RNA 的5-甲基胞嘧啶(m5C)修饰
在多种癌症中发挥作用,NSUN2是m5C甲基转移酶,但它在肝癌中的临床意义、作用机制等尚不明确。
研究方法:
临床样本采集与分组:收集125对肝癌(HCC)及相应癌旁组织(ANL),用于RT-qPCR、western blot及IHC分析NSUN2
表达分布与患者临床特征的相关性,并进行mRNA m5C斑点印迹和m5C-RIP-seq测序。
细胞实验:主要检测多株肝癌细胞株的及增殖、迁移和侵袭等细胞行为学改变。
动物实验:选用5周龄雄性BALB/c裸鼠,在其双侧腋窝皮下接种HCC细胞建立皮下异种移植模型,定期测量肿瘤体积;
通过尾静脉注射HCC细胞建立肺转移模型,用活体成像系统监测转移过程。
其他:RNA免疫沉淀实验、荧光素酶报告基因实验、放线菌素D实验、代谢测量实验等;
主要研究结果:
(1)NSUN2在HCC组织中的表达上调;
通过对125对HCC和癌旁组织(ANL)的研究,运用蛋白质免疫印迹(WB)和免疫组化(IHC)分析,结果显示HCC组织
中NSUN2的蛋白水平显着高于ANL组织。Kaplan-Meier 生存分析,结果显示NSUN2高表达患者的总生存期(OS)和
无复发生存期(RFS)明显低于NSUN2低表达患者。此外,对80例HCC患者的临床病理特征与NSUN2表达进行分析,
发现NSUN2高表达与肿瘤大小、微血管侵犯(MVI)、TNM分期和BCLC分期显着相关。肿瘤越大、存在微血管侵犯、
TNM分期和BCLC分期越晚,NSUN2的表达越高。

图1. HCC组织中NSUN2高表达并与HCC不良预后有关。
(2)体内外实验检测NSUN2 对HCC生长和转移的影响
运用慢病毒分别在HepG2和SNU387细胞中稳定过表达NSUN2,在Hep3B和Huh7细胞中稳定沉默NSUN2。
过表达NSUN2能够促进肝癌细胞增殖和迁移,而沉默NSUN2则抑制肝癌细胞增殖和迁移。体内实验结果表明,
NSUN2过表达显着促进了裸鼠皮下瘤生长并增加肝癌肺转移,而NSUN2沉默则抑制皮下瘤生长和肺转移。

图2. NSUN2在体内外诱导肝癌的生长和转移。
(3)NSUN2介导的m5C修饰在肝癌HCC中的作用
对5对HCC和癌旁正常肝组织进行m5C dot blotting,结果显示HCC组织中总mRNA m5C 水平高于ANL组织;
m5C-RIP-seq分析显示HCC和癌旁正常肝组织m5C修饰存在差异,联合分析mRNA m5C-RIP-seq和 mRNA-Seq数据,
发现HCC中mRNA表达与m5C水平呈轻度正相关;KEGG通路分析显示,表达和m5C水平均上调的mRNA主要富集在
10条信号通路中,其中癌症中的中心碳代谢、半乳糖代谢、果糖和甘露糖
代谢等与代谢相关。

图3. NSUN2介导的m5C高甲基化促进肝细胞癌的代谢转变。
(4)PKM2是NSUN2介导的m5C修饰的主要靶标
对Hep3B-NSUN2-sh2细胞及其阴性对照进行mRNA测序,结果显示敲低NSUN2后,236个基因上调,376个基因下调。
将HCC中表达上调的mRNA、m5C 水平上调的mRNA以及 Hep3B细胞中敲低NSUN2后表达下调的mRNA进行重迭分析,
通过维恩图筛选出11个符合标准的mRNA(B3GNT3、CD7、EML2、FOXC1、GDF15、LRP4、MAPT、MCTP1、PKM2、
PODXL 和 SLC1A7)。检测这11个mRNA在40对HCC和癌旁正常肝组织中的表达,发现其中7个在HCC中上调。
进一步检测这7个mRNA在肝癌细胞系中的表达,结果显示,在HepG2和SNU387细胞中过表达NSUN2后,只有PKM2的表达上调;
在Hep3B 和Huh7细胞中沉默NSUN2后,PKM2的表达下调。此外,根据m5C-RIP-seq结果,
PKM2 mRNA上调的m5C峰位于其3′ - UTR(chr15:72491753 - 72491855,hg19)。通过针对该峰的m5C-RIP-qPCR验证了这一结果,
进一步表明PKM2 mRNA是NSUN2作用的主要靶标。

图4. PKM2 mRNA是NSUN2作用的靶标。
(5)NSUN2通过增加m5C水平稳定PKM2 mRNA
通过放线菌素D处理HCC细胞,并在不同时间点利用RT-qPCR分析PKM2 mRNA水平。结果显示,过表达NSUN2会减缓
PKM2 mRNA的降解,而沉默NSUN2则加速其降解。m5C-RIP-qPCR发现SNU387细胞中过表达NSUN2后,PKM2 mRNA m5C
水平升高;在 Hep3B细胞中沉默NSUN2后,其m5C水平降低;随后,使用针对PKM2的m5C峰的引物和经亚硫酸氢盐转化
RNA逆转录的cDNA模板进行亚硫酸氢盐PCR,然后进行Sanger测序,发现在chr15:72491773(hg19)位点(C773)的信号中,
既有胞嘧啶(‘颁’)又有胸腺嘧啶(‘罢’),这表明该位点在HCC组织和细胞系中均发生了m5C 甲基化。通过计算各样本中
C773位点的m5C水平,发现HCC组织中的m5C水平高于癌旁正常肝组织。同时,SNU387细胞过表达 NSUN2后该位点m5C水平上升,
Hep3B细胞沉默NSUN2后该位点m5C水平则下降。最后,构建含有野生型3′-鲍罢搁的PKM2 mRNA(PKM2-WT)和突变型 C773
(PKM2-Mut)的质粒进行荧光素酶报告基因实验。结果表明,过表达NSUN2可增加 PKM2-WT的荧光素酶活性,对PKM2-Mut
则无此作用;沉默NSUN2的效果则相反表明 NSUN2 对PKM2的调控作用依赖于m5C位点C773。

图5. NSUN2通过增加m5C水平稳定PKM2 mRNA。
(6)NSUN2通过上调PKM2促进HCC的糖酵解和进展
通过检测过表达和敲低NSUN2后HCC细胞的葡萄糖摄取、乳酸生成、细胞外酸化率(ECAR)和糖酵解质子外流率(glycoPER)
来评估糖代谢变化。发现过表达NSUN2显着增加了葡萄糖摄取、乳酸生成、ECAR和glycoPER,敲低NSUN2则降低了这些指标,
表明 NSUN2 促进HCC细胞的糖酵解。
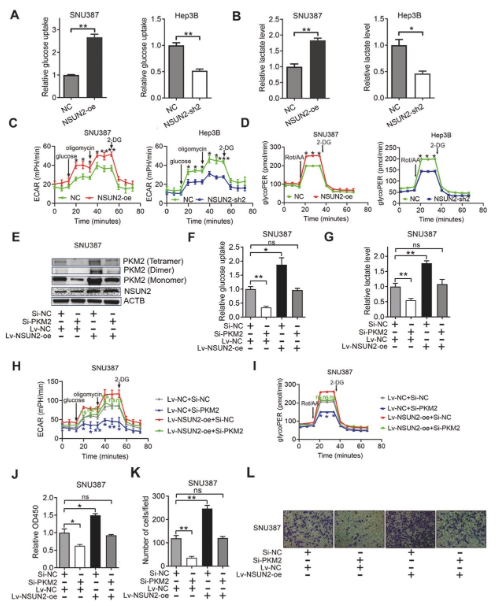
图6. NSUN2通过上调PKM2促进HCC的糖酵解和进展。
随后,使用siRNA靶向PKM2,发现其可下调PKM2四聚体、二聚体和单体的表达,而过表达NSUN2可减缓这种下调作用。
敲低PKM2抑制了葡萄糖摄取、乳酸生成、ECAR和glycoPER,而过表达NSUN2可部分阻断这些抑制作用,表明NSUN2 对
HCC糖酵解的促进作用部分通过上调PKM2实现。最后,检测了PKM2对HCC细胞生长和侵袭的影响及NSUN2的作用,发现
敲低PKM2抑制了HCC细胞的生长和侵袭,而过表达NSUN2可阻断这种抑制作用,说明NSUN2通过上调PKM2促进HCC细胞
的生长和侵袭。
(7)研究示意图
直观地展示从NSUN2表达上调,到PKM2 mRNA稳定、PKM2蛋白增加,再到促进HCC糖酵解、细胞增殖和迁移的一系列过程,
为理解HCC的发病机制提供了重要的理论依据,也为后续研究潜在的治疗靶点提供了方向。

图7. NSUN2介导PKM2在HCC中的m5C调节机制示意图。
研究总结:
肝癌中NSUN2表达上调且与预后不良相关;NSUN2通过增加PKM2 mRNA的m5C修饰稳定其表达,促进糖酵解,进而推动肝癌进展,
研究蝉丑辞耻次明确PKM2是NSUN2介导m5C修饰的靶基因,揭示NSUN2促进肝癌进展的关键机制。综合多种实验方法,从细胞、
动物模型及临床样本辩耻补苍方位验证,NSUN2可作肝癌预后指标和治疗靶点,为肝癌临床诊疗提供新思路。
参考文献
Qi, Q., Zhong, R., Huang, Y. et al. The RNA M5C methyltransferase NSUN2 promotes progression of hepatocellular
carcinoma by enhancing PKM2-mediated glycolysis. Cell Death Dis 16, 82 (2025).
 欢迎来到md传媒官方官网网站!
欢迎来到md传媒官方官网网站! 欢迎来到md传媒官方官网网站!
欢迎来到md传媒官方官网网站!